Étude observationnelle visant à décrire les schémas thérapeutiques de personnes atteintes de cancer du poumon métastatique non à petites cellules avec mutation BRAFV600E (OCTOPUS)
Étude observationnelle visant à décrire les schémas thérapeutiques de personnes atteintes de cancer du poumon métastatique non à petites cellules avec mutation BRAFV600E (OCTOPUS)
Étude observationnelle visant à décrire les schémas thérapeutiques de personnes atteintes de cancer du poumon métastatique non à petites cellules avec mutation BRAFV600E - OCTOPUS
Comment l'essai se déroule-t-il ?
La période d'identification correspond à la période d’éligibilité pour la sélection des participants ayant commencé le traitement en décembre 2017 jusqu’à l’inclusion d’environ 200 patients.
Le schéma ci-dessous présente un résumé de l’étude :
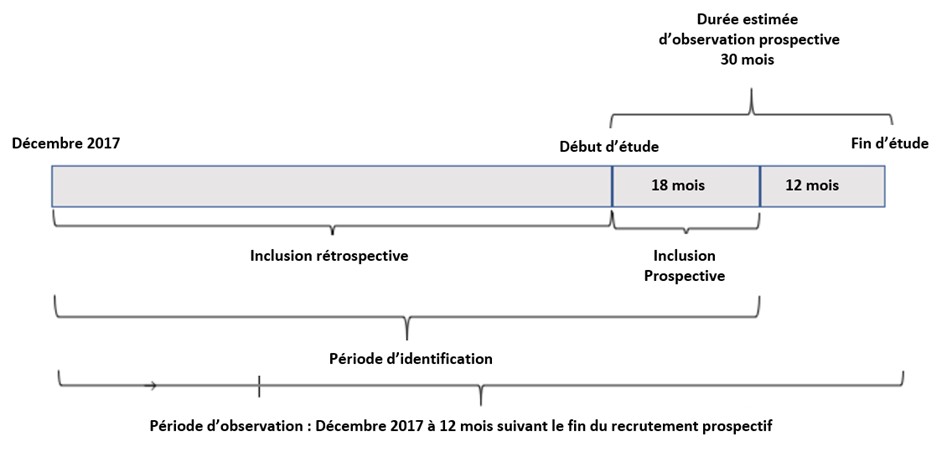
Qui peut participer à cet essai ?
Pour participer à cette étude, les sujets doivent répondre à différents critères, parmi lesquels :
• Être âgé d’au moins 18 ans au moment de l’initiation de la première ligne de traitement pour le CPNPC métastatique.
• Avoir débuté un traitement systémique de première ligne pour le CPNPC métastatique après le 1er décembre 2017.
• Avoir signé un formulaire de consentement éclairé ou de non-opposition à la participation à l’étude.
Quels sont les objectifs de l’essai, et comment sont-ils évalués ?
Le principal objectif de cette étude est de décrire les schémas thérapeutiques des premières et deuxièmes lignes de traitements de participants adultes atteints de CPNPC métastatique avec mutation BRAFV600E.
Les objectifs secondaires de l’étude OCTOPUS sont les suivants :
• Décrire les schémas thérapeutiques pour les lignes de traitement suivantes (postérieures aux premières et deuxièmes lignes).
• Décrire les caractéristiques cliniques et démographiques en recueillant des données telles que l’âge, le genre, les comorbidités, la date de diagnostic initial...
• Décrire l’efficacité des traitements et évaluer l’évolution de la qualité de vie des patients à l’aide de questionnaires.
• Décrire les effets secondaires liés aux traitements de premières et de deuxièmes lignes.
