Essai visant à évaluer l’efficacité et la sécurité de l’association encorafénib, binimétinib et cétuximab chez les patients atteints de cancer colorectal métastatique avec mutation BRAFV600E
Essai visant à évaluer l’efficacité et la sécurité de l’association encorafénib, binimétinib et cétuximab chez les patients atteints de cancer colorectal métastatique avec mutation BRAFV600E

Étude de phase 2 multicentrique en ouvert à bras unique sur l’association encorafénib, binimétinib et cétuximab chez des patients atteints d’un cancer colorectal métastatique avec mutation BRAFV600E n’ayant reçu aucun traitement préalable
Comment l'essai se déroule-t-il ?
Il s’agit d'un essai de phase II en ouvert incluant 95 patients adultes.
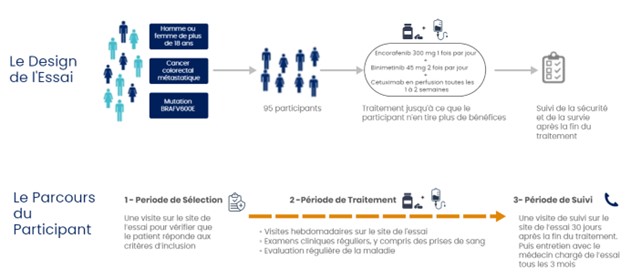
L’essai se déroule en 3 temps :
• Une période de sélection pendant laquelle les patients se rendent à l’hôpital pour vérifier qu’ils répondent aux critères d’inclusion de l’essai.
• Une période de traitement pendant laquelle les patients reçoivent encorafénib, binimétinib et cétuximab jusqu’à ce qu’ils n’en tirent plus de bénéfices. Cela signifie que le traitement sera poursuivi tant que la maladie ne progresse pas et que le traitement est bien toléré. Pendant cette période, les médecins réalisent des examens cliniques, des prises de sang et des examens d'imagerie médicale pour surveiller la taille de la tumeur. Ils vérifient également régulièrement l’état de santé des patients et consignent tout effet secondaire potentiel.
• Une période de suivi qui débute lorsque les patients ont terminé le traitement et consiste à surveiller la santé des patients dans le temps.
Ce schéma synthétise les informations présentées ci-dessus :
Qui peut participer à cet essai ?
Pour participer à cet essai, les patients doivent répondre à différents critères, parmi lesquels :
• Être âgé de 18 ans ou plus et être atteint d’un cancer colorectal qui s'est propagé à d’autres parties du corps (métastatique) avec une mutation du gène BRAF (BRAFV600E).
• Ne pas avoir reçu d’autre traitement pour leur maladie.
Quels sont les objectifs de l’essai, et comment sont-ils évalués ?
Le principal objectif de l’essai est le suivant :
• Evaluer si l’association encorafénib, binimétinib et cétuximab est efficace sur ce type de cancer colorectal. Pour ce faire, on évalue la proportion de patients chez lesquels les tumeurs ont regressé ou disparu après le traitement (taux de réponse objectif).
Cet essai permettra également :
• De déterminer la période pendant laquelle la tumeur continue de répondre au traitement (durée de réponse).
• De déterminer le temps écoulé entre le début du traitement et l’aggravation de la maladie (survie sans progression).
• De déterminer le temps écoulé entre le début du traitement et le décès du patient (survie globale).
• D’évaluer si l’association encorafénib, binimétinib et cétuximab est sûre en analysant le nombre, la fréquence et le type d'effets secondaires.
Quels sont les traitements à l’étude et comment sont-ils administrés ?
Les participants reçoivent les traitements suivants :
• Encorafénib (BRAFTOVI®) : 4 gélules à prendre une fois par jour le matin. La dose quotidienne totale d’encorafénib est de 300 mg.
• Binimétinib (MEKTOVI®) : 3 comprimés deux fois par jour, matin et soir. La dose quotidienne totale de binimétinib est de 90 mg.
• Cétuximab (ERBITUX®) : perfusions en intraveineuse administrées sur le site de l’essai toutes les 1 à 2 semaines.
Durée du traitement : jusqu’à ce que le participant n’en tire plus de bénéfices. Cela signifie que le traitement sera poursuivi tant que la maladie ne progresse pas et que le traitement est bien toléré.
